 È stato appena pubblicato su Science Advances uno studio condotto dal gruppo coordinato da Silvo Conticello, ricercatore dell’Istituto di fisiologia clinica di Pisa (CNR-IFC) e dell’Istituto per lo studio, la prevenzione e la rete oncologica (ISPRO), in collaborazione con Giorgio Mattiuz dell'Università di Firenze: “Evidence for host-dependent RNA editing in the transcriptome of SARS-CoV-2 in humans” di S. Di Giorgio, F. Martignano, M. G. Torcia, G. Mattiuz, S. G. Conticello, https://advances.sciencemag.org/lookup/doi/10.1126/sciadv.abb5813. Nello studio, il sequenziamento dell’RNA del virus, ossia la tecnica usata per calcolare la sequenza dei genomi virali, è stato sfruttato per la prima volta per identificare mutazioni a bassa frequenza, operate dagli enzimi per tentare di attuare il meccanismo di difesa. Anche se il solo editing dell’RNA non è in grado di contrastare l’infezione, averlo individuato mette in evidenza il tallone d’Achille del virus. E lo sviluppo di strumenti in grado di migliorare l’efficienza di quel processo potrebbe gettare le basi per terapie precoci, con un approccio valido non solo contro il Sars-CoV-2, ma anche contro altri tipi di virus. Inoltre, nel breve termine, l’analisi delle mutazioni inserite dagli ADAR e dagli APOBEC può aiutare a individuare regioni del genoma virale importanti per il suo ciclo vitale: quest’informazione può consentire lo sviluppo di terapie mirate per bloccare la replicazione del virus all’interno della cellula.
È stato appena pubblicato su Science Advances uno studio condotto dal gruppo coordinato da Silvo Conticello, ricercatore dell’Istituto di fisiologia clinica di Pisa (CNR-IFC) e dell’Istituto per lo studio, la prevenzione e la rete oncologica (ISPRO), in collaborazione con Giorgio Mattiuz dell'Università di Firenze: “Evidence for host-dependent RNA editing in the transcriptome of SARS-CoV-2 in humans” di S. Di Giorgio, F. Martignano, M. G. Torcia, G. Mattiuz, S. G. Conticello, https://advances.sciencemag.org/lookup/doi/10.1126/sciadv.abb5813. Nello studio, il sequenziamento dell’RNA del virus, ossia la tecnica usata per calcolare la sequenza dei genomi virali, è stato sfruttato per la prima volta per identificare mutazioni a bassa frequenza, operate dagli enzimi per tentare di attuare il meccanismo di difesa. Anche se il solo editing dell’RNA non è in grado di contrastare l’infezione, averlo individuato mette in evidenza il tallone d’Achille del virus. E lo sviluppo di strumenti in grado di migliorare l’efficienza di quel processo potrebbe gettare le basi per terapie precoci, con un approccio valido non solo contro il Sars-CoV-2, ma anche contro altri tipi di virus. Inoltre, nel breve termine, l’analisi delle mutazioni inserite dagli ADAR e dagli APOBEC può aiutare a individuare regioni del genoma virale importanti per il suo ciclo vitale: quest’informazione può consentire lo sviluppo di terapie mirate per bloccare la replicazione del virus all’interno della cellula.
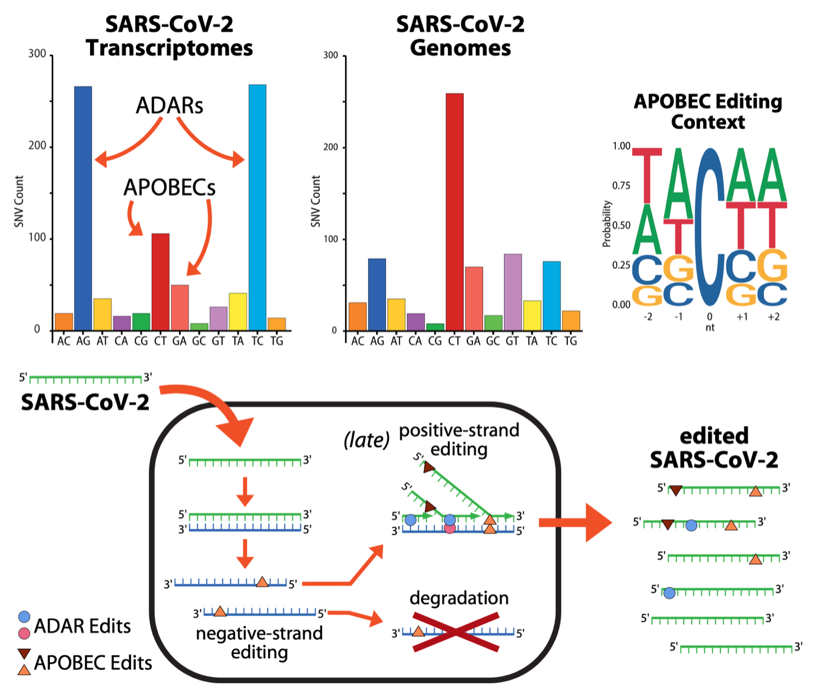
In figura, nei grafici superiori, tra le mutazioni nei trascrittomi e nei genomi virali, sono evidenziate le mutazioni dovute agli ADAR e agli APOBEC, ed, accanto, il particolare tipo di editing dovuto agli APOBEC. Nello schema inferiore è descritto un modello di come potrebbero agire gli ADAR e gli APOBEC durante la replicazione del virus.


 中文
中文  EN
EN 